�Ї�������܊���t(y��)Ժ��3D�����ӡM2���ɼ�(x��)��������ģ�M����M(j��n)Ѫ������
3D�����ӡ�M����ֲ���������t(y��)�W(xu��)�о��ЏV�ǰ���������R���D(zhu��n)�����R�ɴ��������(zh��n)��һ��ֲ������l(f��)�Į��ﷴ��(y��ng)��FBR������(d��o)���w�S��Ĥ�γɺ��װY���m(x��)����K��ֲ���c�����M�����ϣ�����Ѫ�ܻ����㣬�����ֲ��ȱ�������ϵK���о�������������ϵĄ��ȕ��T��(d��o)���ɼ�(x��)�������M1���͘O�����ӄ�FBR�������y(t��ng)��(x��)���������ڴ���y�������L(f��ng)�U���ɱ��ߵȆ��}��
���Q�����y�}���Ї�������܊���t(y��)Ժ�ĸ�С��Ժʿ���ŕ��x���κ��Sɳ�����_�l(f��)��һ�N����M2���ɼ�(x��)��Դ��(x��)��������ģ�M�M2-EVMs���Ą�(chu��ng)�²��ԡ��F(tu��n)�ͨ�^Ĥ�D�����g(sh��)�Ƃ���M2-EVMs��������������īˮ���ӄ�����3D��ӡ֧���У�����M2-EVMs����M1�O�������M(j��n)M2�O����Ѫ�����ɵ����ԣ��p�pFBR�������M��������������Ƥ��ֲ���Ƥ�w����ģ���У����dM2-EVMs��3D��ӡ֧���@���p�����w�S��Ĥ��ȣ�������Ѫ���ܶȺ͂�������Ч�ʣ�չ�F(xi��n)�����õ����������Ժ�����Ч����
���P(gu��n)������“Bioprinted M2 macrophage-derived extracellular vesicle mimics attenuate foreign body reaction and enhance vascularized tissue regeneration”���}�l(f��)���ڡ�Biofabrication���ϡ�

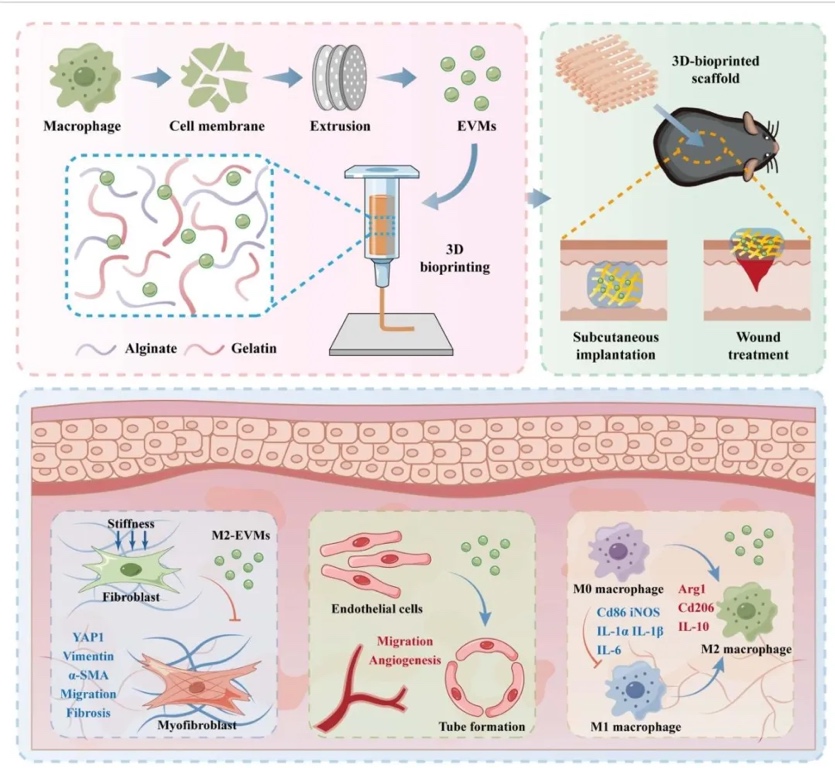
���(n��i)��
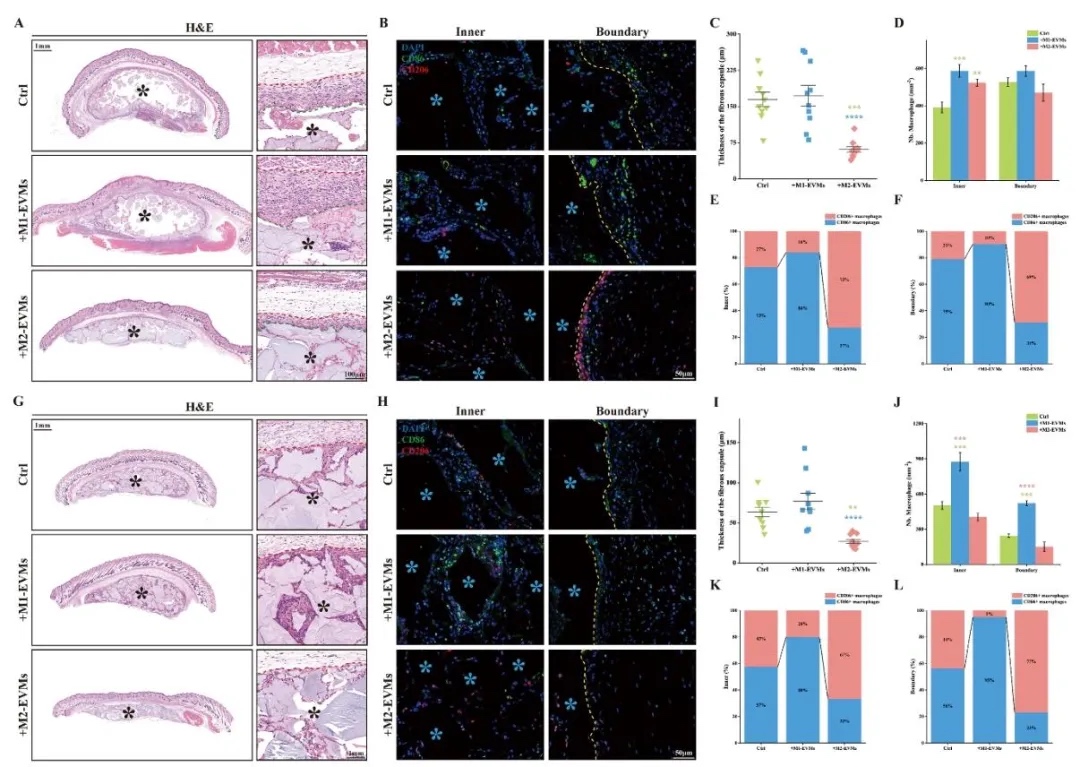
1. 3D�����ӡ֧�܄��Ȍ����ﷴ��(y��ng)��Ӱ푣�ͨ�^Ƥ��ֲ�벻ͬ���ȵ�3D�����ӡ֧�ܣ��Y(ji��)��H&EȾɫ�����ߟɹ⼰�D(zhu��n)䛽M�y���о�֧�܄����c���ﷴ��(y��ng)��FBR�������ɼ�(x��)���O�����P(gu��n)ϵ���Y(ji��)��������Ӳ֧�ܣ�Young’sģ��0.285 MPa���@���T��(d��o)M1���ɼ�(x��)���O����CD86+�����_(d��)80%�����w�S��Ĥ��ȣ�164.7±44.2 µm����ܛ֧�ܵ�3�����Ҵ�������IL-6��TLR4���@�����{(di��o)���C������ͨ�^�ӄ�M1�O������FBR��
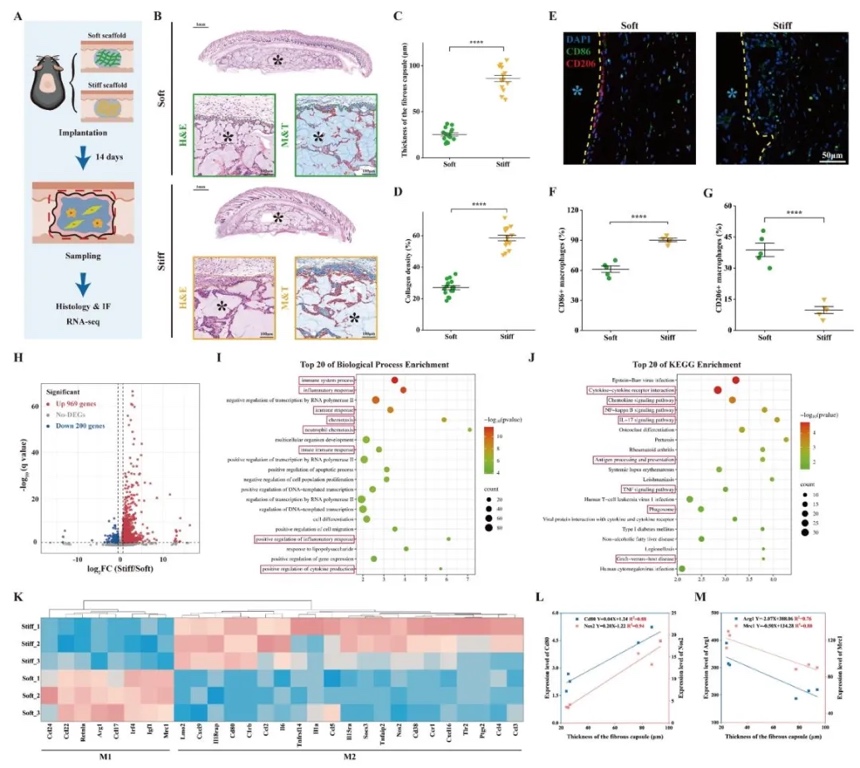
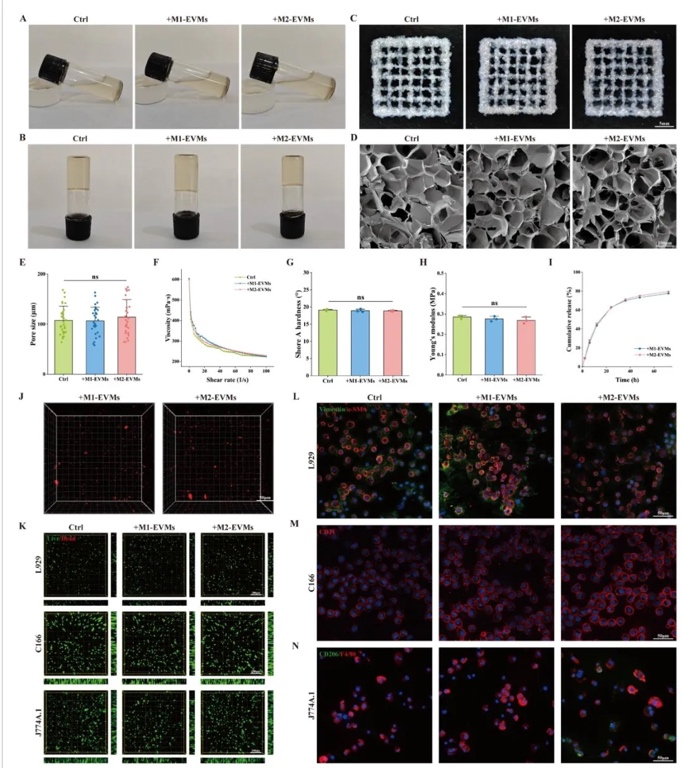
2. M2���ɼ�(x��)��Դ��(x��)��������ģ�M�M2-EVMs�����Ƃ��c����������Ĥ�D�����g(sh��)�Y(ji��)�ϳ�������ݶ��x�ģ��Ƃ���M1/M2-EVMs����ͨ�^HR-TEM��NTA�������|(zh��)ӡ�E������Y(ji��)��(g��u)�ͳɷ֡��Y(ji��)���@ʾ��M2-EVMs�ʈA�����ݽY(ji��)��(g��u)�������s100 nm�����߱��_(d��)M2��(bi��o)ӛ���ף���CD206��Arg1�����ͱ��_(d��)�����ף���TLR4�������ܱ����w�S��(x��)������(n��i)Ƥ��(x��)���;��ɼ�(x��)����Ч�zȡ��6 h��(n��i)�zȡ��>70%����
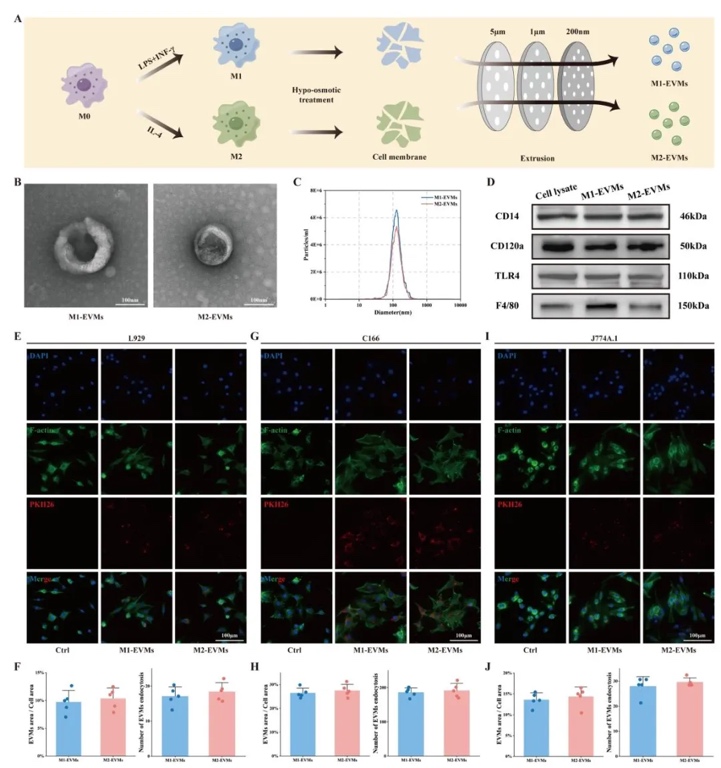
3. M2-EVMs���w�⼚(x��)���О���{(di��o)�����ã�ͨ�^���ی����γɌ�RT-qPCR���о���M2-EVMs�����w�S��(x��)������(n��i)Ƥ��(x��)�������ɼ�(x��)���Ĺ���Ӱ푡��Y(ji��)��������M2-EVMs�@�����Ƴ��w�S��(x��)�����α-SMA���_(d��)����50%�����w�ƣ����M(j��n)��(n��i)Ƥ��(x��)��Ѫ�����ɣ����γɔ�(sh��)������80%�������T��(d��o)���ɼ�(x��)����M2���͘O����CD206+������10%����45%������M1-EVMs�����෴��
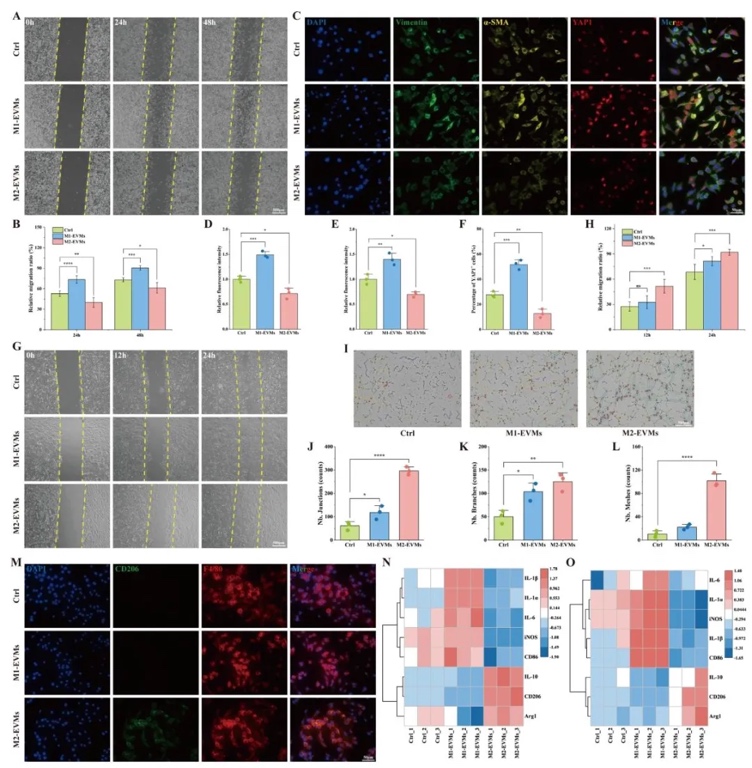
4. ����īˮ�����cEVMsጷ��О飬ͨ�^��׃�W(xu��)�yԇ��SEM��ጷ������������о��˺�EVMs�����z-�������}ˮ���zīˮ�Ĵ�ӡ�m�Ժ�ጷ����ԡ��Y(ji��)��������EVMs����δ�@����׃īˮ�ļ���׃ϡ���ԣ���≈1000 mPa·s���͙Cе���ܣ�Shore AӲ��18.8-19.1°����������72 h��(n��i)���m(x��)ጷţ��۷eጷ���≈80%��������ֲ���֧�ܿ�϶�С�
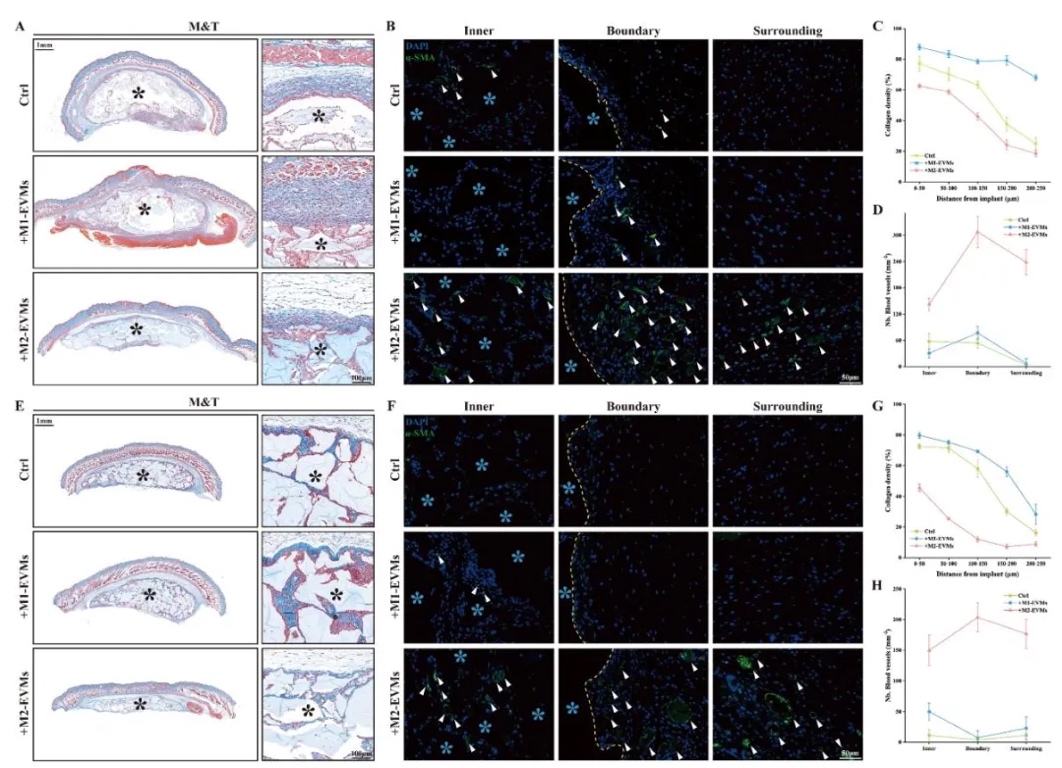
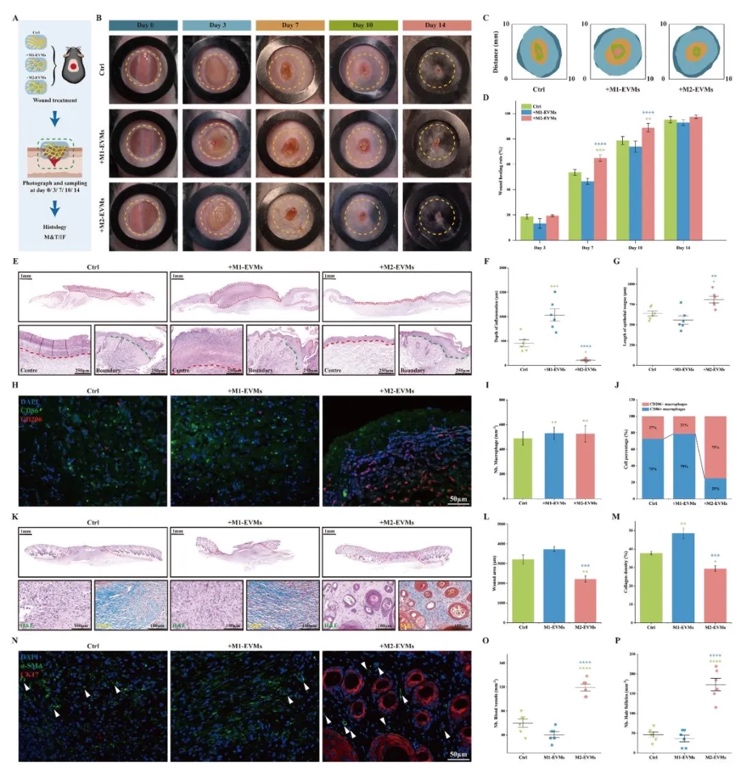
5. ��M2-EVMs��3D�����ӡ֧�ܵ��w��(n��i)�����u����ͨ�^Ƥ��ֲ���ȫ��Ƥ�w����ģ�ͣ��Y(ji��)��H&EȾɫ��MassonȾɫ�����ߟɹ⣬�о���M2-EVMs��FBR�ͽM��������Ӱ푡��Y(ji��)���@ʾ�����dM2-EVMs��Ӳ֧���w�S��Ĥ��ȃH26.7±7.6 µm���^���սM����58%����Ѫ���ܶ�����3������������������40%�������M(j��n)ë�Һ�Ѫ����������M1-EVMs�M�װY����(y��ng)�ӄ���
�о��Y(ji��)Փ
���о��_�l(f��)��һ�N����M2���ɼ�(x��)��Դ��(x��)��������ģ�M�M2-EVMs����3D�����ӡ���ԣ��Խ�Q3D��ӡ�M����ֲ��Į��ﷴ��(y��ng)��FBR����Ѫ�ܻ����㆖�}��ͨ�^Ĥ�D�����g(sh��)�Ƃ��M2-EVMs�����ƾ��ɼ�(x��)�������M1���͘O�������M(j��n)Ѫ���������P(gu��n)���ӷ��ڣ�����Ч�����w�S��(x��)������(n��i)Ƥ��(x��)���zȡ��������������īˮ���ӄ��������z-�������}֧�ܺ�δ�@����׃īˮ�ęCе���ܺʹ�ӡ�m�ԣ����ܳ��m(x��)ጷţ�72 h�۷eጷ���≈80%�����w��(n��i)�����������dM2-EVMs��֧�ܿ�ʹ�w�S��Ĥ��Ƚ���58%��Ѫ���ܶ�����3�����@�����M(j��n)Ƥ�w���ڵ���Ƥ����ë��������Ѫ���γɡ����о��C��M2-EVMsͨ�^�{(di��o)�������h(hu��n)���ʹ��M(j��n)Ѫ�ܻ����@��������3D��ӡ�M���������������������Q�������ֲ�����װY�������y�}�ṩ����;����
����Դ��
https://doi.org/10.1088/1758-5090/add49f
(؟(z��)�ξ���admin)
��һƪ��Nature�ӿ����n���о��F(tu��n)�ʹ��ֱ��īˮ����(DIW)3D��ӡ���g(sh��)�������ܼ���Ʒ
 �K����(li��n)�������W(xu��)Ժ��ĻTo
�K����(li��n)�������W(xu��)Ժ��ĻTo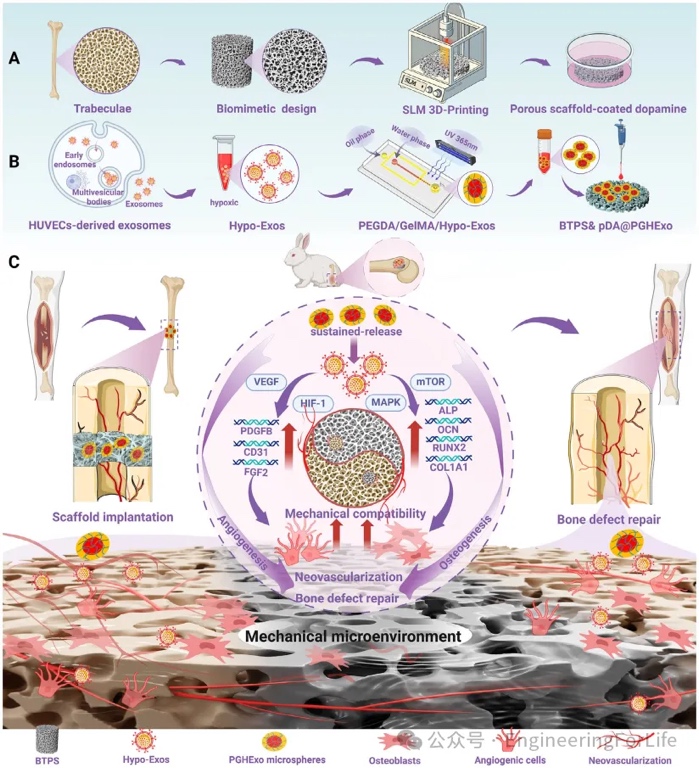 �p�������ԣ�3D��ӡ֧�ܔy
�p�������ԣ�3D��ӡ֧�ܔy �����Z���о��ˆT�l(f��)�F(xi��n)��ÿ
�����Z���о��ˆT�l(f��)�F(xi��n)��ÿ ��(d��ng)����ˮ����Ҋδ���Ƽ���
��(d��ng)����ˮ����Ҋδ���Ƽ��� Nature�ӿ����n���о��F(tu��n)�
Nature�ӿ����n���о��F(tu��n)� �Ї�������܊���t(y��)Ժ��3D
�Ї�������܊���t(y��)Ժ��3D
- ���K����(li��n)�������W(xu��)Ժ��ĻTor Alva������
- ���p�������ԣ�3D��ӡ֧�ܔy�������w����
- �������Z���о��ˆT�l(f��)�F(xi��n)��ÿ�_3D��ӡ�C��
- ����(d��ng)����ˮ����Ҋδ���Ƽ�������˹3D��ӡ
- ��Nature�ӿ����n���о��F(tu��n)�ʹ��ֱ��īˮ
- ���Ї�������܊���t(y��)Ժ��3D�����ӡM2��
- ����cNCDMM����Aheadd CP1���Ƅ��X��
- �����ڽM�������c�����t(y��)�W(xu��)��3D�����ӡˮ
- ���K����(li��n)�������W(xu��)Ժ��ĻTor Alva������
- ���p�������ԣ�3D��ӡ֧�ܔy�������w����
- �������Z���о��ˆT�l(f��)�F(xi��n)��ÿ�_3D��ӡ�C��
- ����(d��ng)����ˮ����Ҋδ���Ƽ�������˹3D��ӡ
- ��Nature�ӿ����n���о��F(tu��n)�ʹ��ֱ��īˮ
- ���Ї�������܊���t(y��)Ժ��3D�����ӡM2��
- ����cNCDMM����Aheadd CP1���Ƅ��X��
- �����ڽM�������c�����t(y��)�W(xu��)��3D�����ӡˮ
- ����e��ԇ�e����������AI�㷨5���i��3D
- �������3D��ӡ-īˮֱ����Nature Review
- ���������ӌW(xu��)��(x��)��ܵ���������TC4��ˇ��
- ���p���Ӿۺϡ��߾��������I(l��ng)��ġ����ǡ�
- ��3D��ӡ����Y(ji��)��(g��u)�O(sh��)Ӌ�K�Oָ�ϣ������p��
- ���C���������·���3D��ӡ���g(sh��)
- ���B�m(x��)�����̼��g(sh��)����ͻ�ƣ�Carbon����
- ��3D�����ӡ���g(sh��)����������ٹ����е���
- ���u݆�~Ƭ�����������������ޏ�(f��)���g(sh��)����
- ���Gɫ�ְ�ȫ��3D��ӡ�zԭˮ���z���IJ���
- ��3D��ӡ�C���g(sh��)���ƴ��FDM��SLA��CLIP��
- ���P�c2024��ʮƪ�l(f��)����Science��Nature


 ͻ��������3D��ӡ
ͻ��������3D��ӡ �ϰ�LEAP 71��˾
�ϰ�LEAP 71��˾ 3D�����ӡ��(g��u)����(n��i)
3D�����ӡ��(g��u)����(n��i) ��Small Science
��Small Science ��������-�����
��������-����� ���A��W(xu��)��������
���A��W(xu��)��������

